医疗质量检测技术展|医疗器械必学法规:医疗器械使用质量监督管理办法(国家食药监管理总局令第18号)

这份法规文件主要规定了医疗器械在使用环节的质量管理要求和监督管理措施,旨在确保医疗器械的使用安全、有效。以下是文件中的关键知识点:
医疗质量检测技术及测试仪器展|实验室质量控制应该怎么做?

为了确保检测数据的准确可靠,以保证检测报告的质量,在检验检测工作中必须有一个质量控制的过程,明确质量控制各阶段可能影响检测报告的各项因素,从而对这些因素采取相应的措施加以管理和控制,以使其过程处于受控状态。实验室需要对哪些内容进行质量控制?
医疗质量检测技术展|机械安全之风险评估究竟怎么搞?

确定了限制,接下来要做危险识别,这个是包括机器全生命周期能想到的危险,所谓全生命周期是指包括运输、装配和安装、试运转、使用、拆卸、停用以及报废的所有阶段。那么,都可能有哪些危险呢?简单概括一下:
医疗质量检测技术及测试仪器展|洁净室验证管理规范

本规范基于《医药工业洁净厂房设计规范》,进一步细化了医疗器械生产洁净室的验证管理要求,特别是设计计划(DQ)、安装验证(IQ)、运行验证(OQ)和性能验证(PQ)四个关键阶段,以确保洁净室的设计、建设、运行均符合GMP及国家相关标准,保障医疗器械的生产质量和安全性。
医疗质量检测技术展|无菌封管机验证指导

从缓冲液和培养基的准备、细胞培养操作、纯化操作到最终配方、过滤和转移,无菌断开是制造过程中的关键要素。
医疗质量检测技术展|有源医疗器械使用期限研究资料在注册过程的常见问题
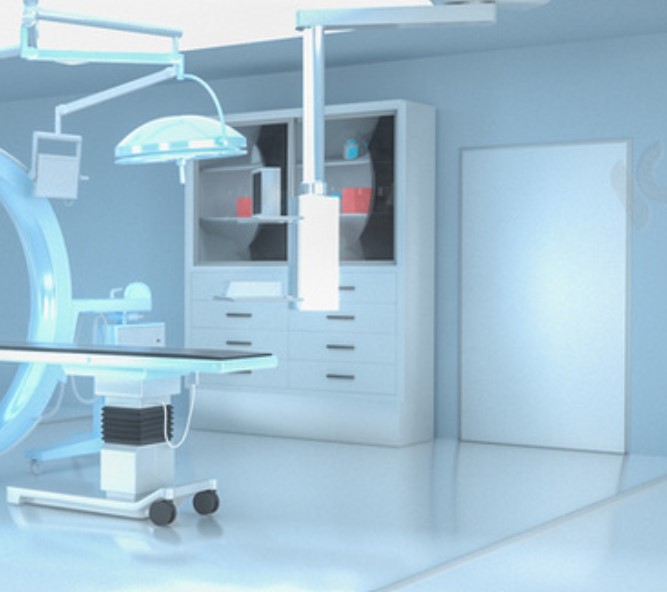
部分申请人在选择直接评价路径时,未对器械的临床应用场景和使用状态进行详细分析,未根据器械结构特点和生产实际设计验证方案。如:低温储存设备、电动病床、洁净工作台等器械结构简单、体型较大,直接对设备整体进行加速试验需要配备大型的恒温恒湿老化试验箱,既增大了试验成本,也给企业自身带来负担,且这类器械主体结构为金属材质,在器械使用期限内较为稳定,不会因失效而产生使用风险。
医疗质量检测技术及测试仪器展|无菌医疗器械包装质量控制要点(上)
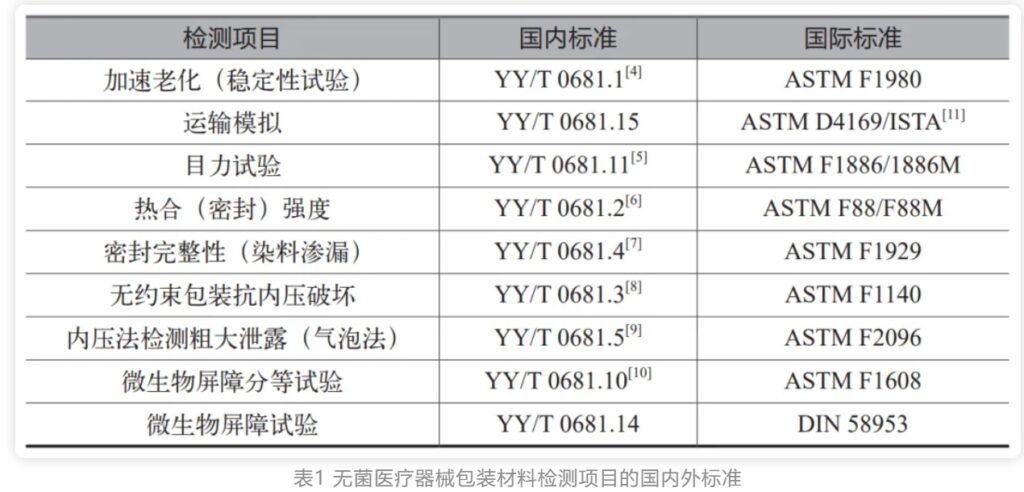
无菌医疗器械包装是保护医疗器械、预防感染的最后一道防线,包装失效会对病人和护士人员的健康和生命带来威胁。无菌医疗器械包装也称为无菌包装屏障系统,不同于食品行业的无菌包装。医疗器械无菌包装不仅需要有阻隔微生物的屏障能力,还要确保灭菌后能在一定期限内维持器械的无菌状态,并能够经受如环氧乙烷、伽马辐照、等离子过氧化氢、蒸汽等方式的灭菌。因此无菌医疗器械包装也被认为是医疗器械组成的一部分。
医疗质量检测技术及测试仪器展|US FDA关于无菌器械灭菌的要求

无菌类器械510(k)中,成熟的灭菌方法包括蒸汽灭菌、干热灭菌、环氧乙烷(EO)灭菌、辐射灭菌、汽化过氧化氢、臭氧等。正在开发的全新灭菌技术并将用于I类和II类器械生产的,被视为新方法。对于采用新灭菌技术灭菌的器械,如果操作不当,会带来灭菌不到位的重大风险。因此,应密切评估使用这些技术灭菌的器械是否符合GMP。FDA计划先审查其制造机构再授予510(k)许可,这将有助于确保器械的安全性和有效性,并降低对人类健康的风险。
医疗质量检测技术及测试仪器展|设计技术考量点
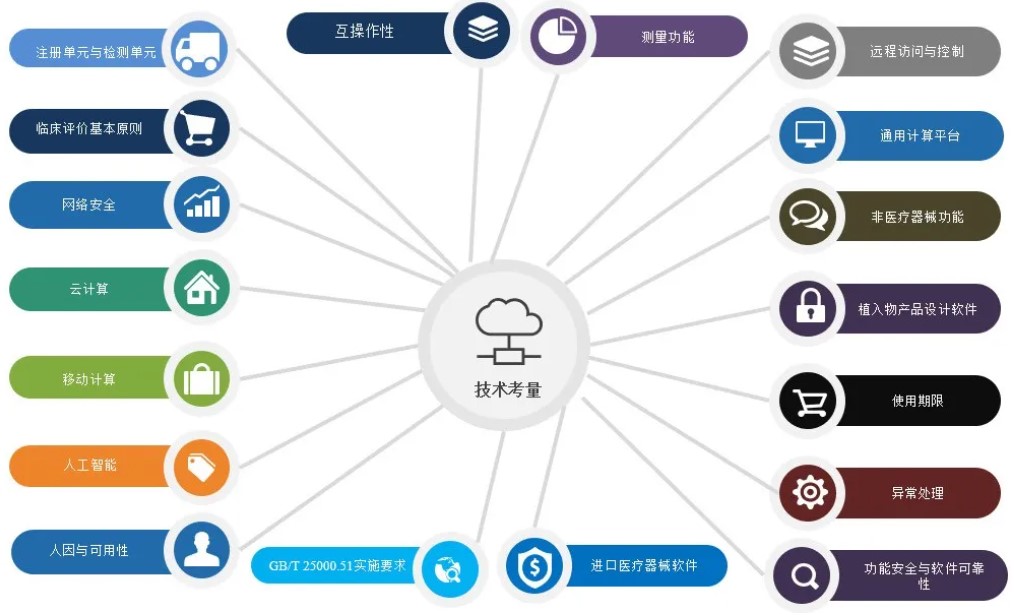
在进行医疗期器械软件设计过程中,我们可以从以下18点来进行技术考量。分别为1.注册单元与检测单元、2.临床评价基本原则、3.网络安全、4.云计算、5.移动计算、6.人工智能、7.人因与可用性、8.互操作性、9.测量功能、10.远程访问与控制、11.通用计算平台、12.非医疗器械功能、13.植入产品设计软件、14.使用期限、15.异常处理、16.功能安全与软件可靠性、17.GB/T25000.51实施要求和18.进口医疗器械软件等要求。
医疗质量检测技术及测试仪器展|医疗器械生物相容性简介、流程、路径和数据
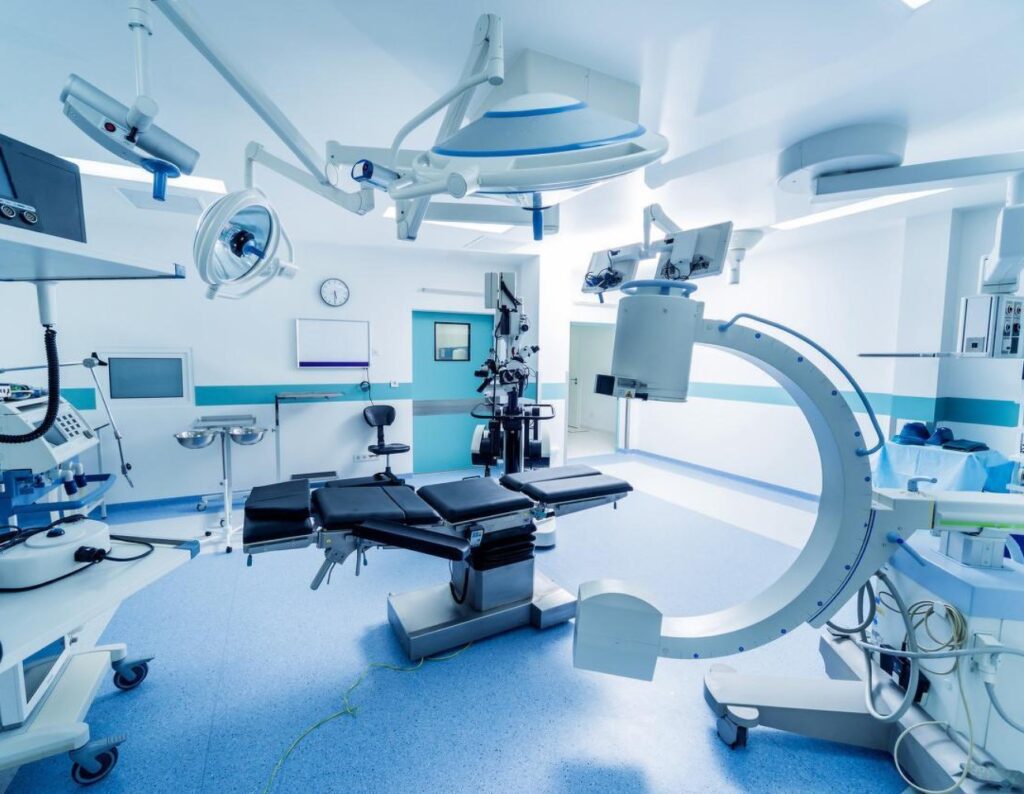
医疗器械生物相容性评价是确保医疗器械安全性和有效性的重要环节,它涉及到对医疗器械在与人体接触时可能产生的生物学反应和风险的全面评估。根据国家标准GB/T 16886.1-2022《医疗器械生物学评价 第1部分:风险管理过程中的评价与试验》,生物相容性评价应作为医疗器械总体评价和开发过程的一部分,贯穿于产品的全生命周期。






