上海医疗检测设备展|无菌医疗器械包装质量控制要点(下)

无菌包装生产技术已经成熟。随着法规和检测技术的不断完善,使用企业对质量要求在逐步提高。法规和质量标准的推出将进一步规范无菌包装产品的质量和性能,从而更好地保障无菌医疗器械的安全性和有效性。
医疗质量检测技术展|包装运输试验和环境试验

国家药监局发布的《医疗器械安全和性能基本原则》中明确规定:医疗器械的设计、生产和包装,包括申请人所提供的说明和信息,应确保在按照预期用途使用时,运输和贮存条件(例如:跌落、振动、温度和湿度的波动)不会对医疗器械的特性和性能,包括完整性和清洁度,造成不利影响。
医疗质量检测技术及测试仪器展|实验室仪器校准周期怎么进行确定?需要参考哪些依据?

实验室内的仪器数量一般都是比较多,在日常校准维护中,需要保持比较合理的周期,定期校准。然后说起仪器校准周期,很多也是老生常谈,常常说是根据仪器使用频繁程度,仪器磨损情况等来确定,但是具体要根据哪些规范做指导,实验室又能不能自己修改校准周期,很多人就不是很清楚。
医疗质量检测技术展|医疗器械必学法规:医疗器械使用质量监督管理办法(国家食药监管理总局令第18号)

这份法规文件主要规定了医疗器械在使用环节的质量管理要求和监督管理措施,旨在确保医疗器械的使用安全、有效。以下是文件中的关键知识点:
医疗质量检测技术展|ISO 13485条款解读、导入与审核(条款5.5.2,管理者代表)

对本条款的审核应围绕条款规定的要求进行,条款要求最高管理者指定一名管理层的成员为管代,“指定”需要具备客观的证据,因此要检查的是否有形成文件的管理者代表任命书。
医疗质量检测技术及测试仪器展|医疗器械独立软件核查中对相关标准的思考
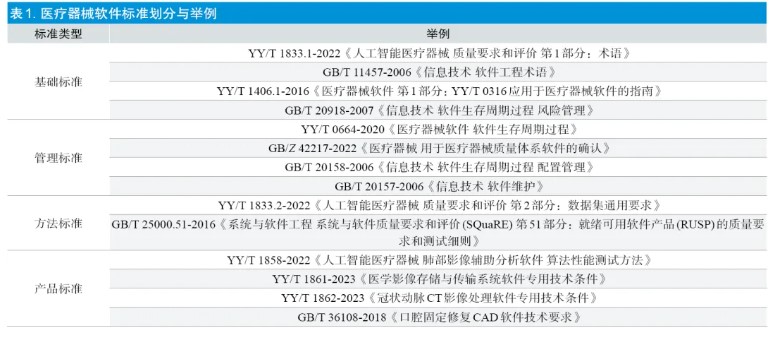
随着计算机技术的进步,医疗器械软件行业正处于高速发展期。近年来,上海市独立软件产品申报数量大幅增长。相较于其他医疗器械产品,软件产品的多样化程度高、技术发展迅速、产品迭代更新快、非实体导致缺陷隐蔽性强,因此产品的安全有效性评价难度较高。在审评核查的过程中发现,医疗器械软件产品常见基本概念不清晰、性能指标和检验方法不明确、产品验证与确认不充分、生存周期过程控制不足等问题。标准在规范产品性能指标、保证产品安全有效性、促进创新和技术进步等方面发挥着重要的作用。随着医疗器械软件行业的迅速发展以及产品自身的复杂性,对配套标准也提出了更高的要求。本文在概要论述医疗器械软件标准发展现状的基础上,分析了目前在医疗器械独立软件审评核查中与标准相关的常见问题,探讨了如何更加有效地开展医疗器械软件质量评价工作,并提出了软件标准未来发展的若干思考和建议,以期加强标准的指导意义、统一评价尺度、促进医疗器械软件的标准化进程。
医疗质量检测技术展|”计量”、”强检”、”检测”

在医疗设备的管理和使用过程中,”计量”、”强检”、和”检测”三个密切相关但又有区别的概念。下面我将为您详细解释这三个术语:
医疗质量检测技术及测试仪器展|医疗器械GMP要升级

2014年12月,原国家食品药品监督管理总局(CFDA)发布了医疗器械生产质量管理规范(以下简称医疗器械GMP)(2014年第64号),并随后陆续推出了无菌医疗器械、植入性医疗器械、体外诊断试剂、定制式义齿和独立软件(注:NMPA发布)等5个附录。
医疗质量检测技术及测试仪器展|实验室质量控制应该怎么做?

为了确保检测数据的准确可靠,以保证检测报告的质量,在检验检测工作中必须有一个质量控制的过程,明确质量控制各阶段可能影响检测报告的各项因素,从而对这些因素采取相应的措施加以管理和控制,以使其过程处于受控状态。实验室需要对哪些内容进行质量控制?
医疗质量检测技术展|收藏!质量体系增加9001后,质量手册调整内容

医疗器械生产监管要求企业建立适应的质量体系以确保产品生产质量可控,但很多企业建立时仅纳入了GMP和13485,后续在做三方认证时意识到了9001的需求,故在原有体系上进行增加9001,这里就质量手册的改动部分做分享






