上海医疗检测设备展|医疗器械注册自检管理规定,那些不知道的细节要点在这里

中国医疗器械行业协会就新修订《医疗器械监督管理条例》及配套规章(上市前)举办了专场培训会,在会上医疗器械注册司的相关领导对《医疗器械注册自检管理规定》进行了相关政策解读。除了正式解读文件,还有尚不清晰的问题不断呈现,针对未理解的部分,医疗器械注册司对细则进行了详细解读。
上海医疗测试仪器展|ISO13485医疗器械质量管理体系认证清单

ISO13485医疗器械质量管理体系认证流程
上海医疗检测设备展|通过医疗设备制造中的质量管理降低风险
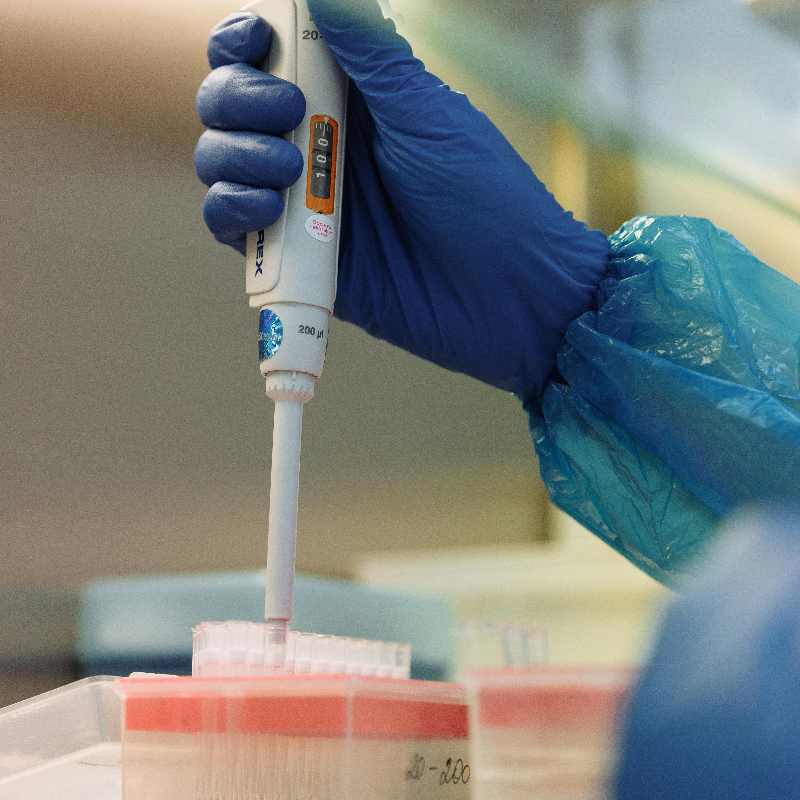
FDA(美国食品和药物管理局)第一级召回或医疗器械公司自愿召回的例子并不鲜见。2019年,美敦力公司(Medtronic)被迫召回1000多台MiniMed胰岛素泵,原因是产品存在网络安全风险,黑客可以遥控操作这些泵。糖尿病患者用胰岛素泵来自我管理胰岛素水平,水平高低关于患者生命健康。
马波斯质量、环境、职业安全健康管理体系再获ISO标准认证

我们高兴地宣布,马波斯已成功通过质量管理体系(ISO 9001)、环境管理体系(ISO 14001)和职业健康与安全管理体系(ISO 45001)的续证审查。
技术论坛G:质量聚焦——助力医疗器械生命周期风险管理
医疗质量检测技术展|医疗器械软件出厂检是不是不需要功能检验?
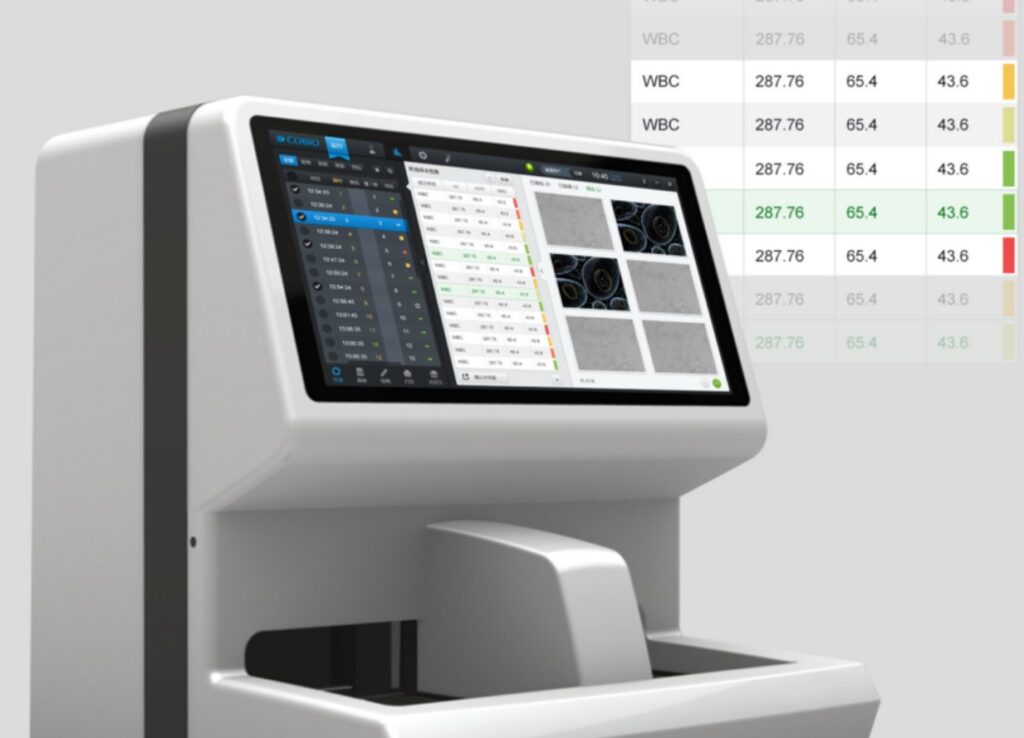
按照《医疗器械生产企业质量控制与成品放行指南》的相关要求,成品检验规程的内容原则上应当覆盖已注册或者备案的产品技术要求中需要常规控制的检验项目和检验方法。对于带软件组件的产品或独立软件,在技术要求中会列出部分软件功能。在设计开发阶段,独立软件已完成功能性能的系统测试验证。在生产阶段基本是一个软件组件的部署或者是独立软件交付物的拷贝过程,在出厂检验中是否可以不对软件功能进行再次测试?
医疗质量检测技术展|医疗器械软件注册检验要点及方法研究
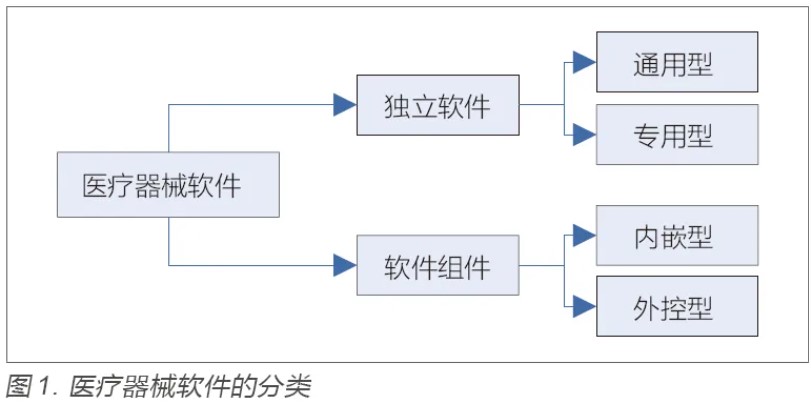
目的:针对医疗器械软件注册检验要点和检测方法进行研究,为加强医疗器械软件的质量保证工作提供参考。方法:以医疗器械软件注册指导原则为基础,梳理不同医疗器械软件的特点和分类,明确软件产品技术要求的编制指南,并且结合通用要求、质量要求、专用要求、安全要求四个方面的要求,对注册检验内容进行解读,最后总结常用检测方法和检测工具。结果:梳理的医疗器械软件注册检验要点可以为注册申请人编写产品技术要求提供指导,总结的检验方法和检测工具可以给检测机构开展相关评测提供借鉴。结论:医疗器械软件检验应从通用要求、质量要求、专用要求和安全要求四个方面进行,检测主要涉及功能测试和性能测试两大类,性能测试通常需借助专业工具进行。
医疗质量检测技术展|人工智能医疗器械注册审查基本原则
人工智能算法的类型不同,其算法特性、适用场景也不同,评价重点亦有所侧重;同时,不同类型的人工智能算法可组合使用,需结合各算法特性和算法组合形式进行整体评价。
医疗质量检测技术及测试仪器展|网络安全更新
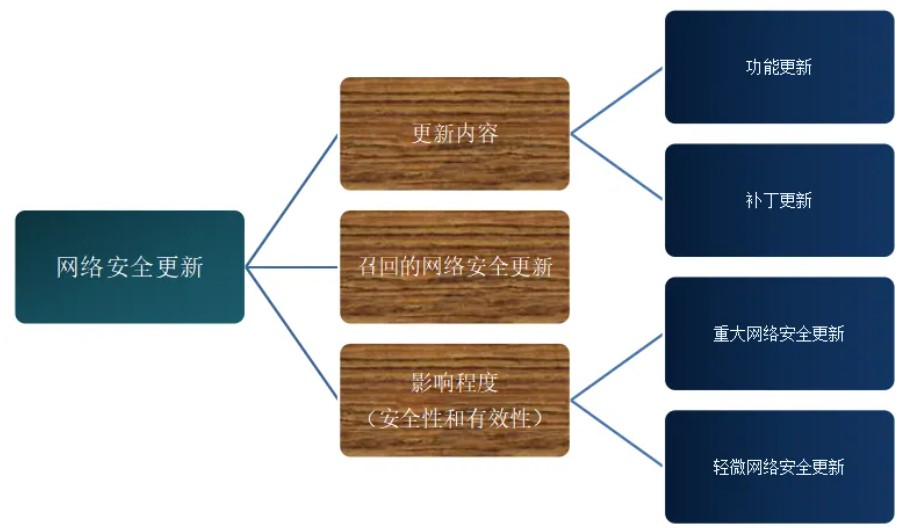
医疗器械网络安全更新从内容上可分为功能更新、补丁更新,类似于增强类软件更新、纠正类软件更新。
根据其对医疗器械安全性和有效性的影响程度分为以下两类:
医疗质量检测技术及测试仪器展|仪器校准后出了校准证书说明仪器合格了?

仪器校准是一门技术活,对于从事生产制造的企业而言,是不可或缺的一环,因为这与产品质量密切相关。所以,了解仪器校准的相关知识也变得尤为重要。






