上海医疗检测设备展|ISO13485和GB/T42061解读、导入与审核(条款7.3.3 设计和开发输入)
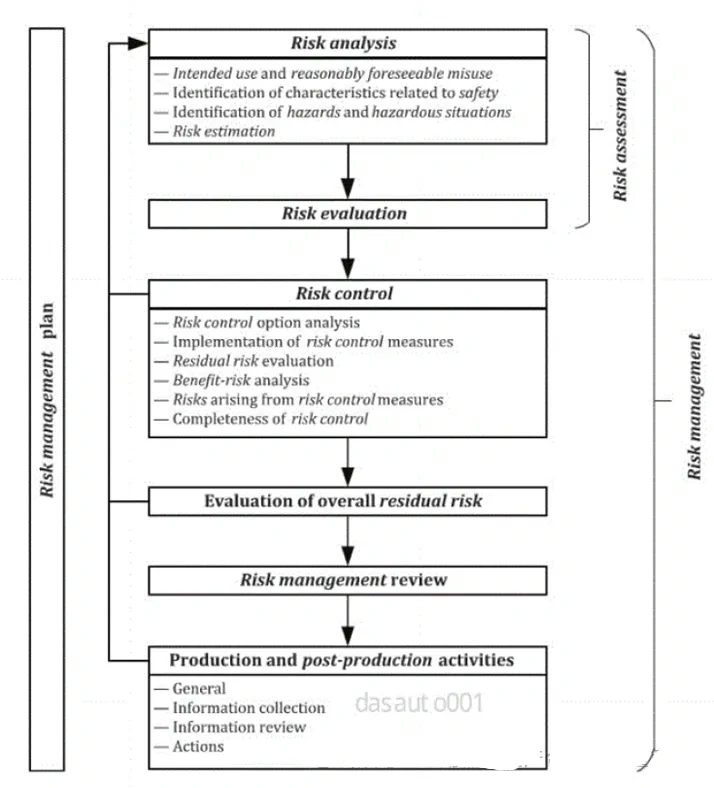
ISO13485:2016《医疗器械质量管理体系用于法规的要求》,由ISO国际标准化组织于2016年3月1 日正式发布,是一项应用于医疗器械领域的质量管理体系的国际标准,强调医疗器械的安全有效,组织提供的医疗器械要满足顾客和法规要求。
医疗质量检测技术展|中国GMP医疗器械生产质量管理规范包含哪些?
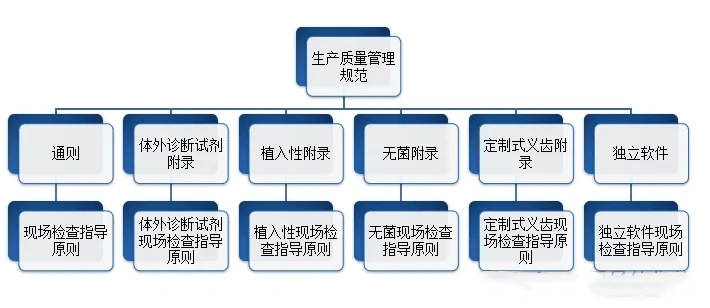
生产企业应当按照医疗器械生产质量管理规范的要求,结合产品特点,建立健全与所生产医疗器械相适应的质量管理体系,并保证其有效运行。在医疗质量检测技术展上,这些生产企业将有机会展示他们如何遵循这些规范,并通过先进的质量管理系统确保其产品的高标准和可靠性。
上海医疗检测设备展l 除菌过滤器的压力监测

《新版GMP附录1:无菌药品》中无菌药品的定义为:无菌药品是指法定药品标准中列有无菌检查项目的制剂和原料药,一般包括注射剂、无菌原料药、眼用制剂、无菌软膏剂、无菌混悬剂等。药品的无菌保证取决于合理且经过验证的灭菌工艺过程、良好的无菌保证体系以及生产过程中严格的GMP管理。
医疗质量检测技术展|浅谈在用医疗器械质量检测的常见方法有哪些

在用医疗器械质量检测的常见方法多种多样,这些方法旨在确保医疗器械的安全性、有效性和符合相关标准。
医疗质量检测技术及测试仪器展|医疗器械GMP要升级

2014年12月,原国家食品药品监督管理总局(CFDA)发布了医疗器械生产质量管理规范(以下简称医疗器械GMP)(2014年第64号),并随后陆续推出了无菌医疗器械、植入性医疗器械、体外诊断试剂、定制式义齿和独立软件(注:NMPA发布)等5个附录。
医疗质量检测技术及测试仪器展|洁净室验证管理规范

本规范基于《医药工业洁净厂房设计规范》,进一步细化了医疗器械生产洁净室的验证管理要求,特别是设计计划(DQ)、安装验证(IQ)、运行验证(OQ)和性能验证(PQ)四个关键阶段,以确保洁净室的设计、建设、运行均符合GMP及国家相关标准,保障医疗器械的生产质量和安全性。
医疗质量检测技术展|有源医疗器械使用期限研究资料在注册过程的常见问题
部分申请人在选择直接评价路径时,未对器械的临床应用场景和使用状态进行详细分析,未根据器械结构特点和生产实际设计验证方案。如:低温储存设备、电动病床、洁净工作台等器械结构简单、体型较大,直接对设备整体进行加速试验需要配备大型的恒温恒湿老化试验箱,既增大了试验成本,也给企业自身带来负担,且这类器械主体结构为金属材质,在器械使用期限内较为稳定,不会因失效而产生使用风险。
医疗质量检测技术及测试仪器展|最终灭菌医疗器械包装材料第5部分:透气材料与塑料膜组成的可密封组合袋和卷材 要求和试验方法
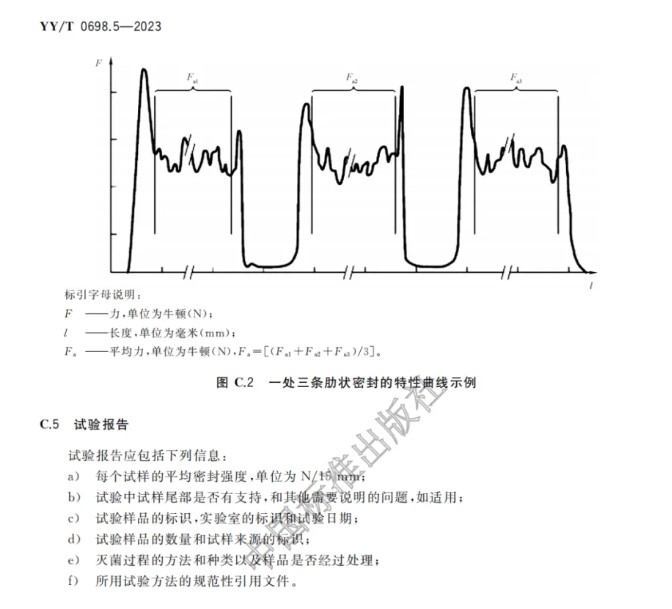
本文件规定了符合YY/T 0698.2、0698.3、0698.6、0698.7、0698.9或 0698.10透气材料和符合本文件第4章规定的塑料膜组成的可密封组合袋和卷材的要求和试验方法。这些可密封组合袋和卷材可用作无菌屏障系统和/或包装系统,以保证最终灭菌医疗器械到使用时的无菌性。
医疗质量检测技术及测试仪器展|医疗器械GMP:检验设备是否都需要校验

企业生产医疗器械时,为确认产品性能指标以及生产和检验环境的洁净度,需要对产品性能指标、洁净区环境、工艺用水、产品无菌性能、环氧乙烷残留量(EO灭菌)等进行检验。质量检验的结果是否准确可靠,取决于检验设备测量的结果的准确性,企业在使用检验设备时,需要提供客观证据,证明设备符合要求。
医疗质量检测技术展|医疗器械注册检验常见问题答疑汇总

A:维氏硬度检测不需要提供单独的试样,在送检样品上取样测试;洛氏硬度检测若被测部位形状不规则时,无法直接对样品进行测试,应提供原材料试样块,并提供材质、热处理工艺一致性声明。






