技术资讯
仪器校准以后,在仪器校准机构出具完校准证书以后,就会在所校准的仪器上贴上校准标签,校准标签上会有此次校准相关的信息,这些信息是提供给设备管理人员溯源以及巡查的参考,以方便相关人员 陈知道仪器上一次具体的校准情况信息,那么仪器校准标签有哪些常见错误?检查这几点就可以了。
仪器,校准

仪器校准以后,在仪器校准机构出具完校准证书以后,就会在所校准的仪器上贴上校准标签,校准标签上会有此次校准相关的信息,这些信息是提供给设备管理人员溯源以及巡查的参考,以方便相关人员 陈知道仪器上一次具体的校准情况信息,那么仪器校准标签有哪些常见错误?检查这几点就可以了。
仪器,校准
对于普通消费者而言,越来越多的人开始发现UDI的存在却并不了解其意义。但对于医疗器械从业者而言,UDI早已进入视野多年,UDI不仅仅只是一个专有名词,更是一个对生命健康有效监管的预警保障,也是从业者需要积极认识并应用实施的必备工具。
UDI,标识

对于普通消费者而言,越来越多的人开始发现UDI的存在却并不了解其意义。但对于医疗器械从业者而言,UDI早已进入视野多年,UDI不仅仅只是一个专有名词,更是一个对生命健康有效监管的预警保障,也是从业者需要积极认识并应用实施的必备工具。
UDI,标识
在进行医疗期器械软件设计过程中,我们可以从以下18点来进行技术考量。分别为1.注册单元与检测单元、2.临床评价基本原则、3.网络安全、4.云计算、5.移动计算、6.人工智能、7.人因与可用性、8.互操作性、9.测量功能、10.远程访问与控制、11.通用计算平台、12.非医疗器械功能、13.植入产品设计软件、14.使用期限、15.异常处理、16.功能安全与软件可靠性、17.GB/T25000.51实施要求和18.进口医疗器械软件等要求。
质量管理,设计
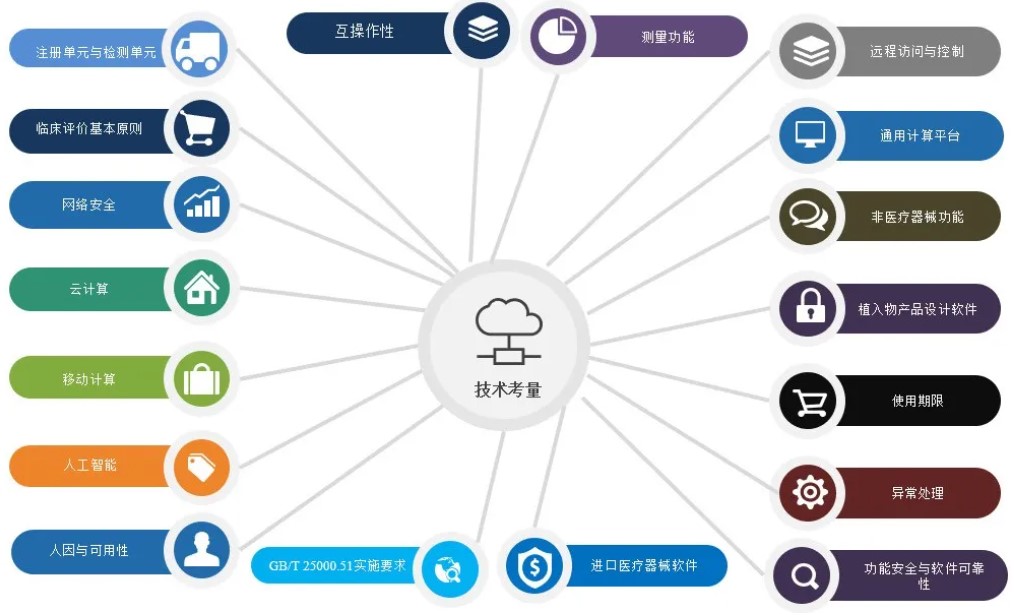
在进行医疗期器械软件设计过程中,我们可以从以下18点来进行技术考量。分别为1.注册单元与检测单元、2.临床评价基本原则、3.网络安全、4.云计算、5.移动计算、6.人工智能、7.人因与可用性、8.互操作性、9.测量功能、10.远程访问与控制、11.通用计算平台、12.非医疗器械功能、13.植入产品设计软件、14.使用期限、15.异常处理、16.功能安全与软件可靠性、17.GB/T25000.51实施要求和18.进口医疗器械软件等要求。
质量管理,设计
对于拟使用的同品种医疗器械非公开数据等需要提供授权,以保证数据来源的合法性;使用公开发表的数据,如公开发表的文献、数据、信息等,不需取得授权。数据如果来自公开数据、试验测量、行业共识等,不需取得授权。
质量管理,授权
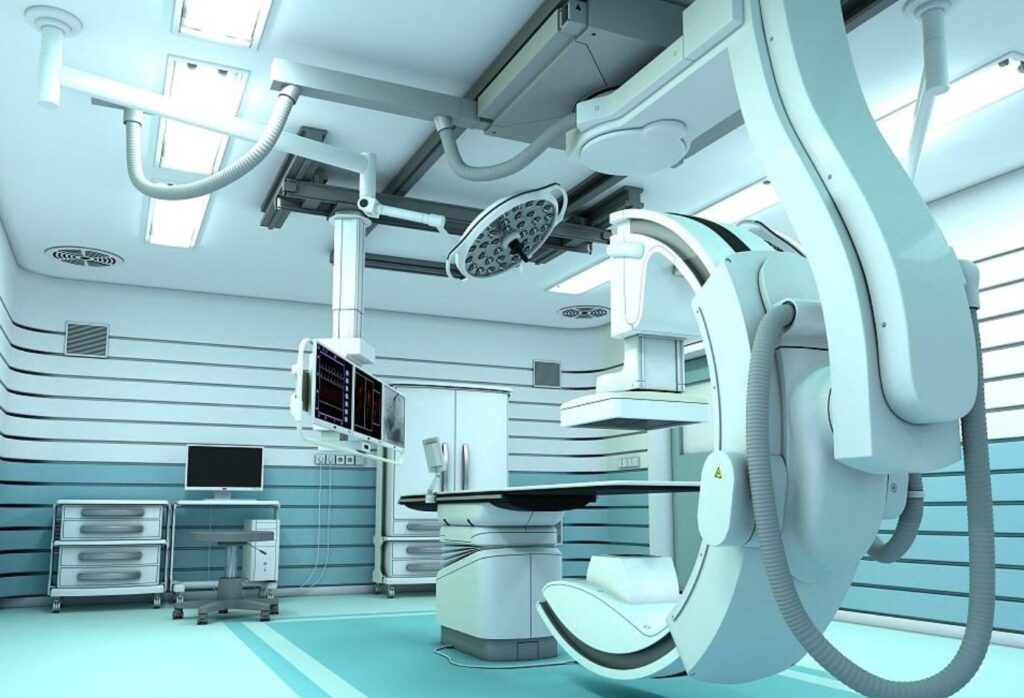
对于拟使用的同品种医疗器械非公开数据等需要提供授权,以保证数据来源的合法性;使用公开发表的数据,如公开发表的文献、数据、信息等,不需取得授权。数据如果来自公开数据、试验测量、行业共识等,不需取得授权。
质量管理,授权
测试完成后,您将需要制作一份可用性工程报告,该报告需要提交给您的医疗设备销售市场的相应监管机构。需要注意的是,这份报告不应该简单地总结你的可用性验证测试,而是需要一个非常具体的格式。
可用性测试
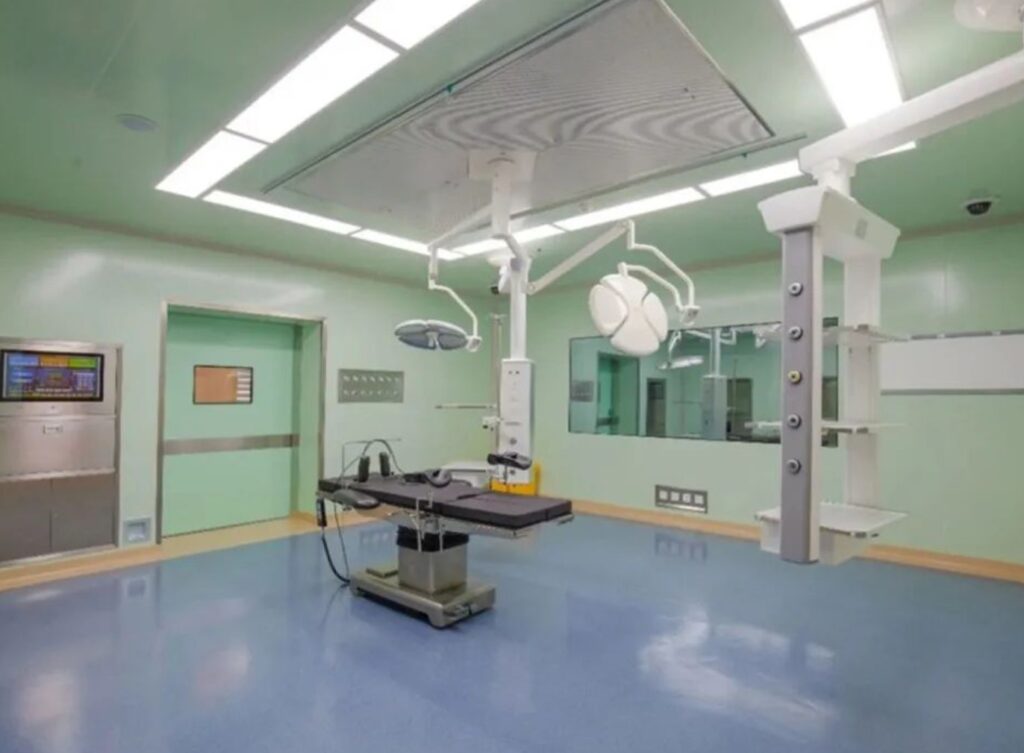
测试完成后,您将需要制作一份可用性工程报告,该报告需要提交给您的医疗设备销售市场的相应监管机构。需要注意的是,这份报告不应该简单地总结你的可用性验证测试,而是需要一个非常具体的格式。
可用性测试
技术资讯
近日,欧盟MDCG发布《隐形眼镜Master UDI-DI解决方案的实施指南》,在结构、分配、标签和注册等方面为隐形眼镜实施Master UDI-DI规则提供指引。
UDI, 标识

近日,欧盟MDCG发布《隐形眼镜Master UDI-DI解决方案的实施指南》,在结构、分配、标签和注册等方面为隐形眼镜实施Master UDI-DI规则提供指引。
UDI, 标识

本次测试依据[详细的测试标准,如 IEC 60601-1:2005 等相关标准及具体条款]对医疗器械产品进行耐压测试,以确保产品在正常使用及可能的异常电气条件下,其绝缘性能能够保障使用者的安全,防止电击事故发生。
耐压测试

本次测试依据[详细的测试标准,如 IEC 60601-1:2005 等相关标准及具体条款]对医疗器械产品进行耐压测试,以确保产品在正常使用及可能的异常电气条件下,其绝缘性能能够保障使用者的安全,防止电击事故发生。
耐压测试
水质污染的核心因素:季节变化(温度、微生物) 农业污染(农药、化肥、无机物) 工业污染(有机物) 生活污染(排泄物、微生物) 市政水消毒(氨与氯的化合物) 用户总进水(施工带来的污染)
实践, 用水3Q4, 验证

水质污染的核心因素:季节变化(温度、微生物) 农业污染(农药、化肥、无机物) 工业污染(有机物) 生活污染(排泄物、微生物) 市政水消毒(氨与氯的化合物) 用户总进水(施工带来的污染)
实践, 用水3Q4, 验证







