首页 » 行业资讯
行业新闻
- 2024-08-07
近期国家药监局在对部分医疗器械企业进行飞检过程中,发现部分企业的质量管理体系存在较大缺陷,本次笔者就针对飞检的2家企业的问题进行收集整理,希望对各企业在质量管理体系的管理中有所借鉴和帮助。
案例, 质量管理, 飞行检查

近期国家药监局在对部分医疗器械企业进行飞检过程中,发现部分企业的质量管理体系存在较大缺陷,本次笔者就针对飞检的2家企业的问题进行收集整理,希望对各企业在质量管理体系的管理中有所借鉴和帮助。
案例, 质量管理, 飞行检查

- 2024-08-06
DQE是在产品设计和开发过程中负责质量管理和质量保证的专业人员。他们的主要职责是确保产品设计符合质量标准和客户要求。以下是DQE设计质量工程师的常见工作职责:
1. 质量计划和策略:制定和执行产品设计和开发阶段的质量计划和策略,确保产品符合质量标准和规范。
岗位职责, 质量管理
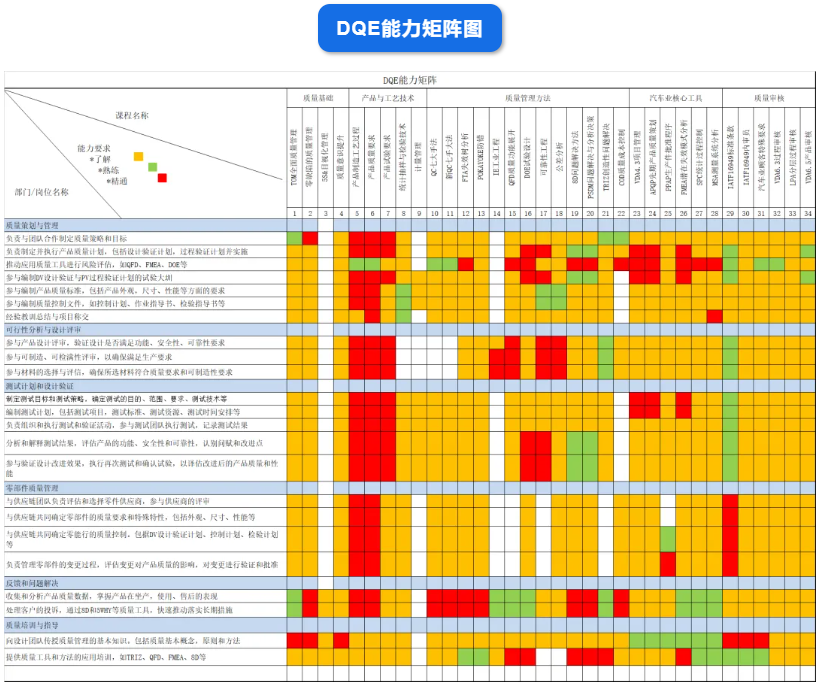
DQE是在产品设计和开发过程中负责质量管理和质量保证的专业人员。他们的主要职责是确保产品设计符合质量标准和客户要求。以下是DQE设计质量工程师的常见工作职责:
1. 质量计划和策略:制定和执行产品设计和开发阶段的质量计划和策略,确保产品符合质量标准和规范。
岗位职责, 质量管理
- 2024-08-06
焦距是光学系统的一个非常重要的指标,对于焦距的概念,大家或多或少都有了解,我们这里再回顾一下。
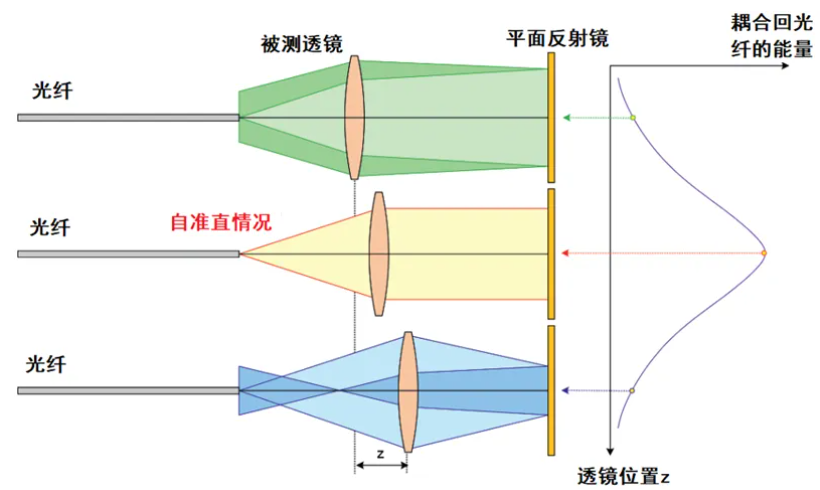
光学系统的焦距,定义为平行光入射时从光学系统的光学中心到光束聚焦点的距离,是衡量光学系统中光的聚集或发散的度量方式。我们用下面的图来说明这一概念。
光学, 测试, 质量管理
焦距是光学系统的一个非常重要的指标,对于焦距的概念,大家或多或少都有了解,我们这里再回顾一下。
光学系统的焦距,定义为平行光入射时从光学系统的光学中心到光束聚焦点的距离,是衡量光学系统中光的聚集或发散的度量方式。我们用下面的图来说明这一概念。
光学, 测试, 质量管理
行业新闻
- 2024-10-14
洁净室与周围的空间必须维持一定的压差,并应按工艺要求决定维持正压差,通常情况洁净度高的区域流向洁净度低的区域,使洁净室的洁净度不受到污染空气的干扰。
控制, 洁净室
洁净室与周围的空间必须维持一定的压差,并应按工艺要求决定维持正压差,通常情况洁净度高的区域流向洁净度低的区域,使洁净室的洁净度不受到污染空气的干扰。
控制, 洁净室
- 2024-10-14
无菌包装生产技术已经成熟。随着法规和检测技术的不断完善,使用企业对质量要求在逐步提高。法规和质量标准的推出将进一步规范无菌包装产品的质量和性能,从而更好地保障无菌医疗器械的安全性和有效性。
包装质量, 控制

无菌包装生产技术已经成熟。随着法规和检测技术的不断完善,使用企业对质量要求在逐步提高。法规和质量标准的推出将进一步规范无菌包装产品的质量和性能,从而更好地保障无菌医疗器械的安全性和有效性。
包装质量, 控制
- 2024-09-24
国家药监局发布的《医疗器械安全和性能基本原则》中明确规定:医疗器械的设计、生产和包装,包括申请人所提供的说明和信息,应确保在按照预期用途使用时,运输和贮存条件(例如:跌落、振动、温度和湿度的波动)不会对医疗器械的特性和性能,包括完整性和清洁度,造成不利影响。
试验

国家药监局发布的《医疗器械安全和性能基本原则》中明确规定:医疗器械的设计、生产和包装,包括申请人所提供的说明和信息,应确保在按照预期用途使用时,运输和贮存条件(例如:跌落、振动、温度和湿度的波动)不会对医疗器械的特性和性能,包括完整性和清洁度,造成不利影响。
试验
- 2024-09-24
实验室内的仪器数量一般都是比较多,在日常校准维护中,需要保持比较合理的周期,定期校准。然后说起仪器校准周期,很多也是老生常谈,常常说是根据仪器使用频繁程度,仪器磨损情况等来确定,但是具体要根据哪些规范做指导,实验室又能不能自己修改校准周期,很多人就不是很清楚。
仪器校准

实验室内的仪器数量一般都是比较多,在日常校准维护中,需要保持比较合理的周期,定期校准。然后说起仪器校准周期,很多也是老生常谈,常常说是根据仪器使用频繁程度,仪器磨损情况等来确定,但是具体要根据哪些规范做指导,实验室又能不能自己修改校准周期,很多人就不是很清楚。
仪器校准
- 2024-09-24
这份法规文件主要规定了医疗器械在使用环节的质量管理要求和监督管理措施,旨在确保医疗器械的使用安全、有效。以下是文件中的关键知识点:
管理办法, 质量监督

这份法规文件主要规定了医疗器械在使用环节的质量管理要求和监督管理措施,旨在确保医疗器械的使用安全、有效。以下是文件中的关键知识点:
管理办法, 质量监督






