上海医疗检测设备展|无菌医疗器械包装质量控制要点(下)

无菌包装生产技术已经成熟。随着法规和检测技术的不断完善,使用企业对质量要求在逐步提高。法规和质量标准的推出将进一步规范无菌包装产品的质量和性能,从而更好地保障无菌医疗器械的安全性和有效性。
医疗质量检测技术及测试仪器展|无菌医疗器械包装质量控制要点(上)
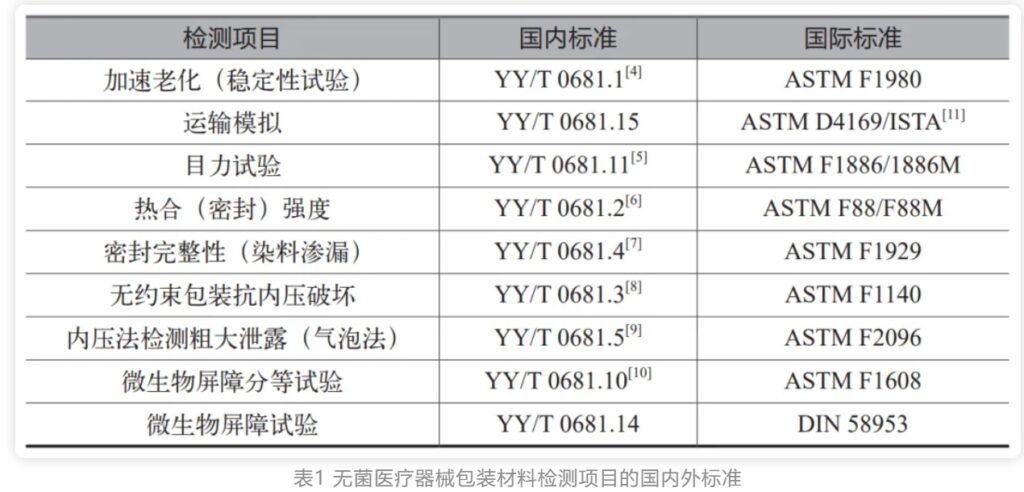
无菌医疗器械包装是保护医疗器械、预防感染的最后一道防线,包装失效会对病人和护士人员的健康和生命带来威胁。无菌医疗器械包装也称为无菌包装屏障系统,不同于食品行业的无菌包装。医疗器械无菌包装不仅需要有阻隔微生物的屏障能力,还要确保灭菌后能在一定期限内维持器械的无菌状态,并能够经受如环氧乙烷、伽马辐照、等离子过氧化氢、蒸汽等方式的灭菌。因此无菌医疗器械包装也被认为是医疗器械组成的一部分。
医疗质量检测技术展|医疗器械“体考”到底是什么?

《医疗器械生产监督管理办法》明确规定:医疗器械生产企业应当按照医疗器械生产质量管理规范的要求,建立质量管理体系并保持有效运行。申请人在申请产品注册时,受理注册申请的药品监督管理部门在产品技术审评时,认为有必要对质量管理体系进行核查的,会组织开展质量管理体系核查。
医疗质量检测技术展|医疗器械注册质量管理体系核查指南介绍

本指南旨在加强医疗器械注册质量管理体系的核查管理,确保核查工作的质量。依据包括《医疗器械监督管理条例》、《医疗器械注册与备案管理办法》、《体外诊断试剂注册与备案管理办法》、《医疗器械生产监督管理办法》、《医疗器械生产质量管理规范》、《医疗器械临床试验质量管理规范》及《医疗器械注册自检管理规定》等法规。
上海医疗测试仪器展|ISO13485医疗器械质量管理标准 问与答 (一)

医疗器械质量管理体系起源于2000年我国发布的第22号医疗器械质量管理体系核查要求,并在此基础上历经九年发展形成了我国第一版医疗器械生产质量管理规范。随着医疗器械行业的快速发展,我国于2014年对GMP进行了修正并形成了最新的标准规范。同时,其他国家和地区也陆续建立了相应的质量管理体系标准法规,例如美国的CDMP及后续QSF20法规,欧盟的ENISO13485标准及其多次修订等。在70年代,美国率先制定了CDMP法规,并在其基础上于1996年发布针对质量管理体系要求的QSF20法规。欧盟则从1993年开始酝酿并报告了EN1N46001标准法规,但后来对该标准进行了修订和完善。国际标准化组织在1996年发布了基于ISO9001系列的两个医疗器械质量管理体系标准,即ISO13485:1996版与ISO13481:1996版,并随9001版本升级不断调整优化,最终在2016年发布了全新的ISO13485:2016版标准。
医疗质量检测技术展|质量部DQE、SQE、CQE、PQE 岗位职责有哪些?
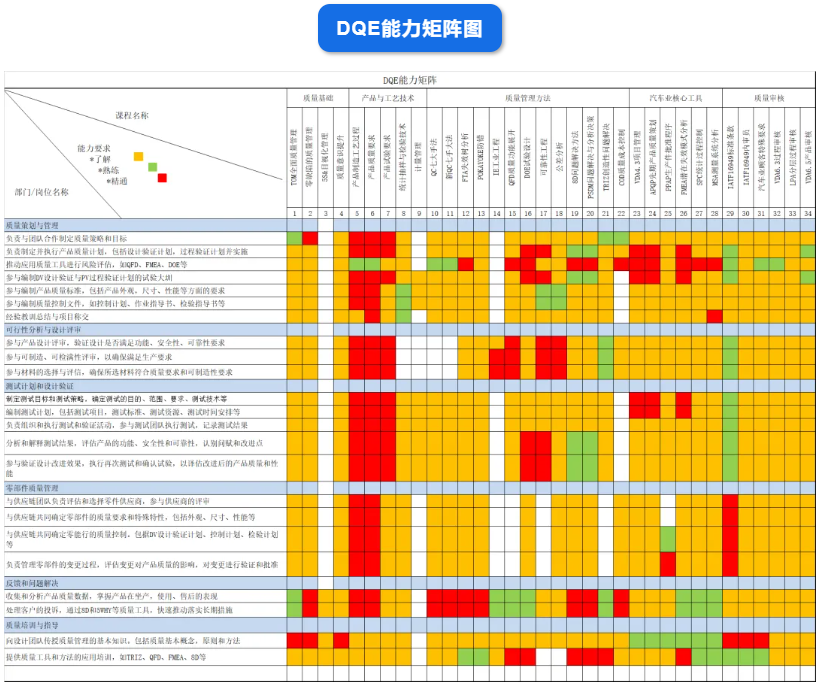
DQE是在产品设计和开发过程中负责质量管理和质量保证的专业人员。他们的主要职责是确保产品设计符合质量标准和客户要求。以下是DQE设计质量工程师的常见工作职责:
1. 质量计划和策略:制定和执行产品设计和开发阶段的质量计划和策略,确保产品符合质量标准和规范。
医疗器械行业展览|减轻医疗器械供应链中的产品责任风险

当身处错综复杂的全球化时代,当网络支配着所有的商业脉搏,当患者因医疗器械产品组件故障而受伤,当不熟悉供应链中的所有环节,结果将令人望而生畏。
医疗质量检测技术及测试仪器展 | 一大波国内外领先的质量检测供应商来袭!来Medtec 2024现场一探究竟(二)

医疗质量检测技术及测试仪器展本文整理了部分企业的展品预览,快来一睹为快吧~
上海医疗检测设备展|张纲:标准化——新质生产力发展的引擎

4月26日,2024中关村论坛标准化与科技创新发展平行论坛在京举办。原国务院参事,中国标准化专家委员会副主任委员张纲在会上以“高标准引领新质生产力发展”为题发表主旨演讲。上海医疗检测设备展小编了解到,在会后,张纲参事将演讲内容进一步整理,形成本文。《中国标准化》以署名文章形式全文刊载,以飨读者。
医疗质量检测技术展|五部门印发!强化计量、检验检测、认证认可等质量要素
为贯彻落实党的二十大精神和《质量强国建设纲要》部署要求,提升产业链供应链韧性和安全水平,培育战略性新兴产业,抢占未来产业发展先机,加快传统产业转型升级,促进建设现代化产业体系,现就发挥质量基础设施效能、助力产业链供应链质量联动提升,提出如下意见。






