医疗质量检测技术展|医械生物相容性评价的目标和方法

根据ISO 10993-1:2018的定义,生物相容性是指医疗器械或材料在一个特定应用中引起恰当宿主反应的能力。“生物相容”与“生物不相容”不是某种材料天然的或绝对的“标签”,而是需要结合材料的具体性能和特定的(临床)应用场景进行判断。同时,生物相容性是一个动态概念,植入物植入人体后会对特定生物组织环境产生物理和化学影响,引起生物学反应;反之,生物组织也会对植入物产生影响,使之发生物理或化学变化,两者的相互作用会一直持续。即使植入物被完全去除或被人体完全吸收,其影响还将持续一段时间。
医疗质量检测技术展|医疗器械生物相容性评价介绍

医疗器械生物相容性评价是一个复杂而细致的过程,它要求对医疗器械的各个方面进行全面考量。随着科技的发展和标准的完善,生物相容性评价将继续发展,以确保医疗器械的安全性和有效性,保护患者的健康。
医疗器械生物相容性评价

生物相容性作为保障医疗器械安全性的一个重要指标,其研究分析必须贯穿项目的始终,占据了大量财力、精力和时间。很多行业人员谈“生物相容性”即色变,其实懂得了原理,生物相容性评价也很简单。医疗器械立项、研发等早期的过程中,生物相容性所需要的成本,基本上可以转移至上游供应商,要求他们提供相应的证明资料,并签订质量协议规定供方的责任和风险。
医疗质量检测技术及测试仪器展|无菌医疗器械包装质量控制要点(上)
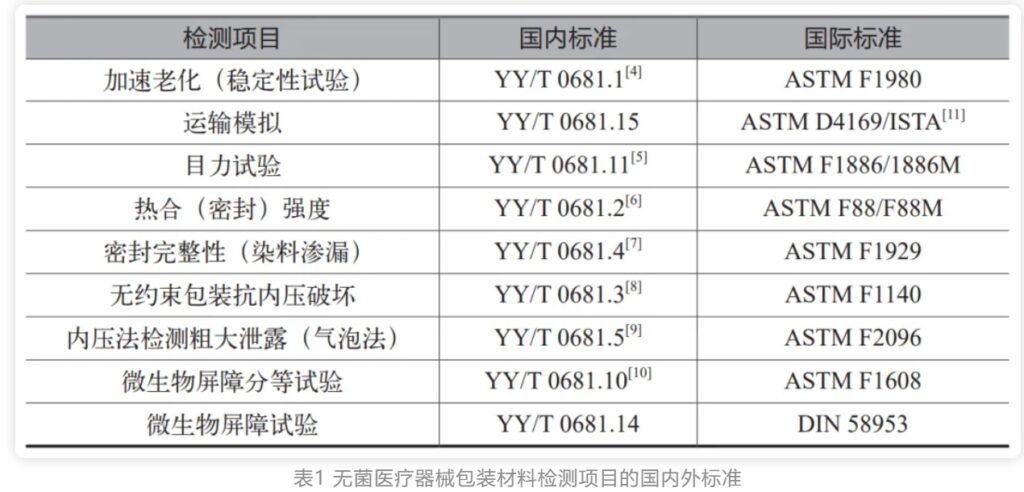
无菌医疗器械包装是保护医疗器械、预防感染的最后一道防线,包装失效会对病人和护士人员的健康和生命带来威胁。无菌医疗器械包装也称为无菌包装屏障系统,不同于食品行业的无菌包装。医疗器械无菌包装不仅需要有阻隔微生物的屏障能力,还要确保灭菌后能在一定期限内维持器械的无菌状态,并能够经受如环氧乙烷、伽马辐照、等离子过氧化氢、蒸汽等方式的灭菌。因此无菌医疗器械包装也被认为是医疗器械组成的一部分。
医疗质量检测技术展|医疗器械原材料变更的基本流程

医疗器械的预期用途、技术要求、安全有效性、有效期等等,很大程度上取决于原材料。
产品注册时确定下来的原材料,轻易不能变化。
但是,企业在实际经营过程中,常常为了降低成本、改善某方面性能、完善供应链、符合升版的标准,或主动、或被动地对原材料进行变更。
医疗质量检测技术及测试仪器展|医疗器械生物相容性简介、流程、路径和数据
医疗器械生物相容性评价是确保医疗器械安全性和有效性的重要环节,它涉及到对医疗器械在与人体接触时可能产生的生物学反应和风险的全面评估。根据国家标准GB/T 16886.1-2022《医疗器械生物学评价 第1部分:风险管理过程中的评价与试验》,生物相容性评价应作为医疗器械总体评价和开发过程的一部分,贯穿于产品的全生命周期。
医疗质量检测技术及测试仪器展 | 浅谈吻(缝)合器外科产品技术评审要点
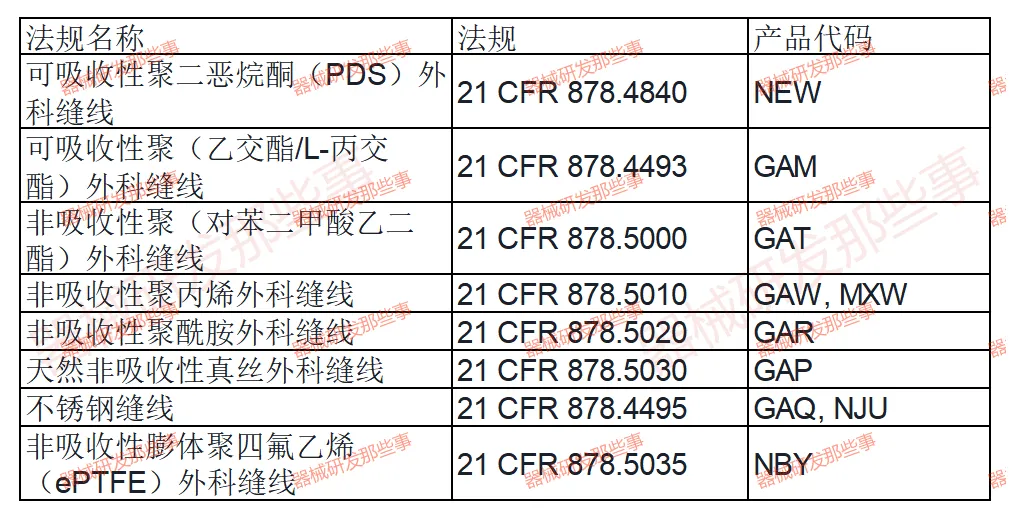
吻(缝)合器外科产品在临床手术中扮演着至关重要的角色,其安全性、有效性和可靠性直接关系到患者的生命健康。
医疗质量检测技术及测试仪器展 | 一大波国内外领先的质量检测供应商来袭!来Medtec 2024现场一探究竟(一)
医疗质量检测技术及测试仪器展整理了部分质量检测展品预览,快来一睹为快吧~






