医疗质量检测技术及测试仪器展|质量管理体系构建中,值得避坑的案例学习!

近期国家药监局在对部分医疗器械企业进行飞检过程中,发现部分企业的质量管理体系存在较大缺陷,本次笔者就针对飞检的2家企业的问题进行收集整理,希望对各企业在质量管理体系的管理中有所借鉴和帮助。
医疗质量检测技术及测试仪器展|浅谈有源医疗器械技术审评关注点
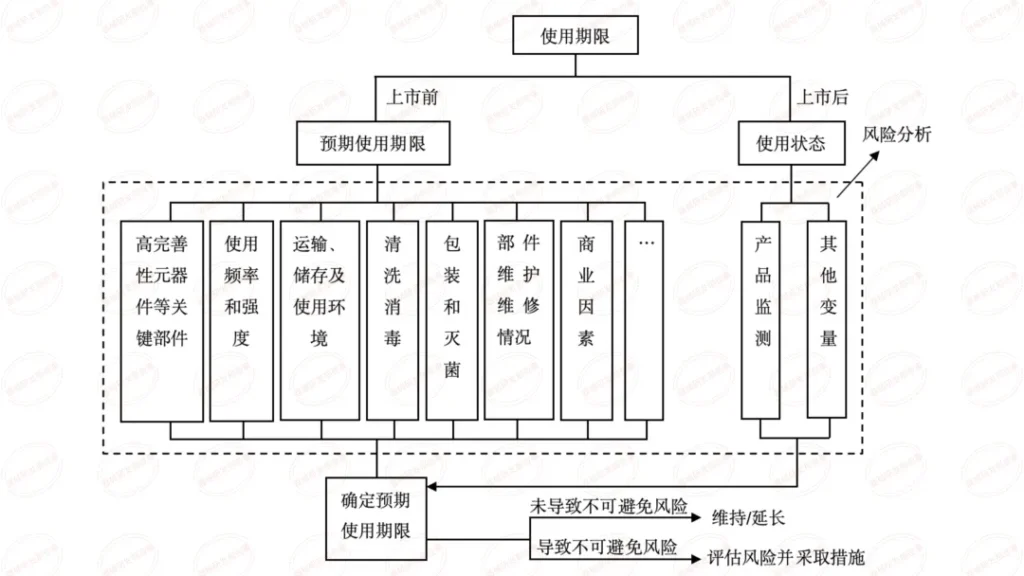
本篇内容为学习总结,源自审评二部陈敏老师关于《有源医疗器械注册申报资料要求及常见问题介绍》在器审中心学习云课程的视频。陈老师主要介绍了共性问题、研究资料-联合使用、研究资料-生物学特性、研究资料-清洁、消毒、灭菌、稳定性和92个技术审评共性问题等六个方面。
上海医疗检测设备展|ISO13485和GB/T42061解读、导入与审核(条款7.3.3 设计和开发输入)
ISO13485:2016《医疗器械质量管理体系用于法规的要求》,由ISO国际标准化组织于2016年3月1 日正式发布,是一项应用于医疗器械领域的质量管理体系的国际标准,强调医疗器械的安全有效,组织提供的医疗器械要满足顾客和法规要求。
医疗质量检测技术展|医疗器械注册检验常见问题答疑汇总

A:维氏硬度检测不需要提供单独的试样,在送检样品上取样测试;洛氏硬度检测若被测部位形状不规则时,无法直接对样品进行测试,应提供原材料试样块,并提供材质、热处理工艺一致性声明。
上海医疗检测设备展|医疗器械认证过程中的风险管理要点

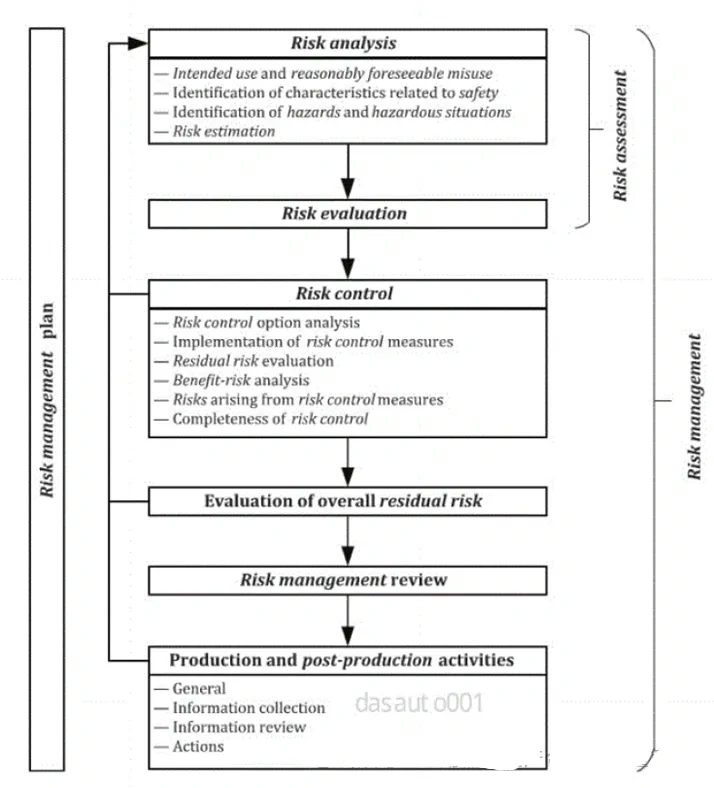
当我们谈论医疗器械行业的风险管理时,有些人可能会认为这是一个令人生畏的混乱过程。一开始可能会让人不知所措,但这对确保我们开发的器械在整个生命周期内安全有效至关重要。这不仅仅是为了满足监管要求—虽然这绝对是其中的一部分—而是为了做出明智的决策,保护患者并降低器械失效的可能性。
上海医疗检测设备展|【专访】安徽英太自动化科技有限公司-总经理 马华伟先生

安徽英太自动化科技有限公司以全球检漏市场为导向,立足于气密检漏仪、气密检漏系统的研发、生产及销售并提供一站式的气密检漏解决方案。
医疗质量检测技术展|深入解析MDR下的高质量临床随访调查(Level 4 PMCF Surveys)

随着欧盟医疗器械法规(MDR)的实施,对医疗设备行业的监管要求日益严格。CE认证的持续持有,需要制造商持续进行市场后评估、临床数据收集和证据生成。本文将深入探讨MDR下的高质量临床随访调查(Level 4 PMCF Surveys),为制造商提供实用的指导和建议。
上海医疗测试仪器展|医疗器械中的风险管理与可用性测试

医疗器械的可用性测试是指通过代表性用户使用器械并执行具有代表性的任务,以此来揭示器械的交互优点和改进机会。其目的是了解器械是否满足用户需求,最关键的是能否满足安全操作的需求。通过设计更改,达到设计改善和设计确认的目的,确认其不会造成危险性使用失误。
上海医疗检测设备展|2022-2027年检验检测行业全景调研及投资策略分析报告
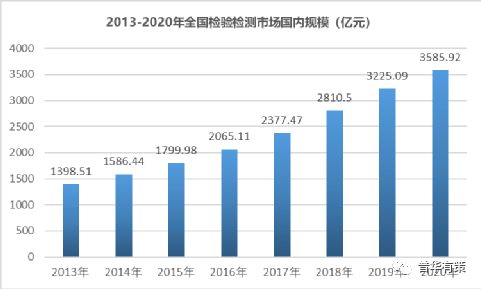
第三方检测服务的基本商业运作逻辑,是第三方检测服务机构以独立于供需双方(如供应商与采购商、销售商与消费者)、监管双方(如政府与企业)的第三方身份进行检测活动,在供需双方、监管双方之间传递质量可靠的信息,从而消除各主体间的信息不对称,优化监管过程、交易过程并降低其成本。
医疗质量检测技术展|大模型引领检验检测认证新未来

随着人工智能技术的发展,大模型在各个领域都展示出强大的应用潜力。本文分析了大模型技术在检验检测认证领域的典型应用场景,展望了大模型技术在检验检测认证领域的发展方向,以期为大模型在检验检测认证领域的应用提供借鉴。






