医疗质量检测技术展|FDA推荐使用的医疗器械CVSS标准

CVSS是一种普遍适用的风险评分框架,广泛用于IT和信息安全领域,帮助企业评估并优先处理各类漏洞
医疗质量检测技术及测试仪器展|医疗器械独立软件核查中对相关标准的思考
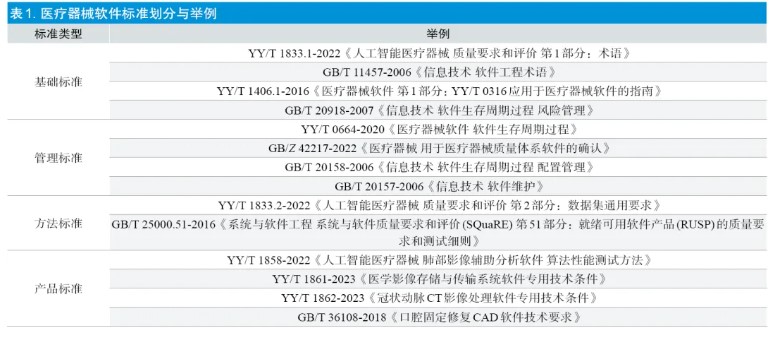
随着计算机技术的进步,医疗器械软件行业正处于高速发展期。近年来,上海市独立软件产品申报数量大幅增长。相较于其他医疗器械产品,软件产品的多样化程度高、技术发展迅速、产品迭代更新快、非实体导致缺陷隐蔽性强,因此产品的安全有效性评价难度较高。在审评核查的过程中发现,医疗器械软件产品常见基本概念不清晰、性能指标和检验方法不明确、产品验证与确认不充分、生存周期过程控制不足等问题。标准在规范产品性能指标、保证产品安全有效性、促进创新和技术进步等方面发挥着重要的作用。随着医疗器械软件行业的迅速发展以及产品自身的复杂性,对配套标准也提出了更高的要求。本文在概要论述医疗器械软件标准发展现状的基础上,分析了目前在医疗器械独立软件审评核查中与标准相关的常见问题,探讨了如何更加有效地开展医疗器械软件质量评价工作,并提出了软件标准未来发展的若干思考和建议,以期加强标准的指导意义、统一评价尺度、促进医疗器械软件的标准化进程。
医疗质量检测技术及测试仪器展|读懂GB9706医疗器械强制标准,离不开这5大问题!

GB9706.1-2020《医用电气设备 第1部分:基本安全和基本性能的通用要求》已经从2023年5月1日起开始实施。那么,企业在执行GB9706系列标准时经常遇到哪些问题?久顺收集汇总不少企业相关询问,本期一并解答。
上海医疗测试仪器展|ISO13485医疗器械质量管理标准 问与答 (一)

医疗器械质量管理体系起源于2000年我国发布的第22号医疗器械质量管理体系核查要求,并在此基础上历经九年发展形成了我国第一版医疗器械生产质量管理规范。随着医疗器械行业的快速发展,我国于2014年对GMP进行了修正并形成了最新的标准规范。同时,其他国家和地区也陆续建立了相应的质量管理体系标准法规,例如美国的CDMP及后续QSF20法规,欧盟的ENISO13485标准及其多次修订等。在70年代,美国率先制定了CDMP法规,并在其基础上于1996年发布针对质量管理体系要求的QSF20法规。欧盟则从1993年开始酝酿并报告了EN1N46001标准法规,但后来对该标准进行了修订和完善。国际标准化组织在1996年发布了基于ISO9001系列的两个医疗器械质量管理体系标准,即ISO13485:1996版与ISO13481:1996版,并随9001版本升级不断调整优化,最终在2016年发布了全新的ISO13485:2016版标准。
上海医疗检测设备展|金属材料|| 金属材料盐雾试验检测原理、检测步骤及标准方法汇总

盐雾测试是一种主要利用盐雾试验设备所创造的人工模拟盐雾环境条件来考核产品或金属材料耐腐蚀性能的环境试验。它分为两大类,一类为天然环境暴露试验,另一类为人工加速模拟盐雾环境试验。
上海医疗检测设备展|张纲:标准化——新质生产力发展的引擎

4月26日,2024中关村论坛标准化与科技创新发展平行论坛在京举办。原国务院参事,中国标准化专家委员会副主任委员张纲在会上以“高标准引领新质生产力发展”为题发表主旨演讲。上海医疗检测设备展小编了解到,在会后,张纲参事将演讲内容进一步整理,形成本文。《中国标准化》以署名文章形式全文刊载,以飨读者。
马波斯质量、环境、职业安全健康管理体系再获ISO标准认证

我们高兴地宣布,马波斯已成功通过质量管理体系(ISO 9001)、环境管理体系(ISO 14001)和职业健康与安全管理体系(ISO 45001)的续证审查。
分论坛2:质量提升与体系、标准建设
一文了解医疗器械放射治疗设备行业标准知识

该标准对放射性粒子植入治疗计划系统的长度重建偏差、体积重建偏差、剂量计算偏差、剂量场分布准确性进行了规定。具体来说,长度重建偏差不大于2mm,体积重建偏差不大于10%,剂量计算偏差不大于10%,剂量分布面积重合率不小于90%。
医疗质量检测技术及测试仪器展|浅谈有源医疗器械技术审评关注点
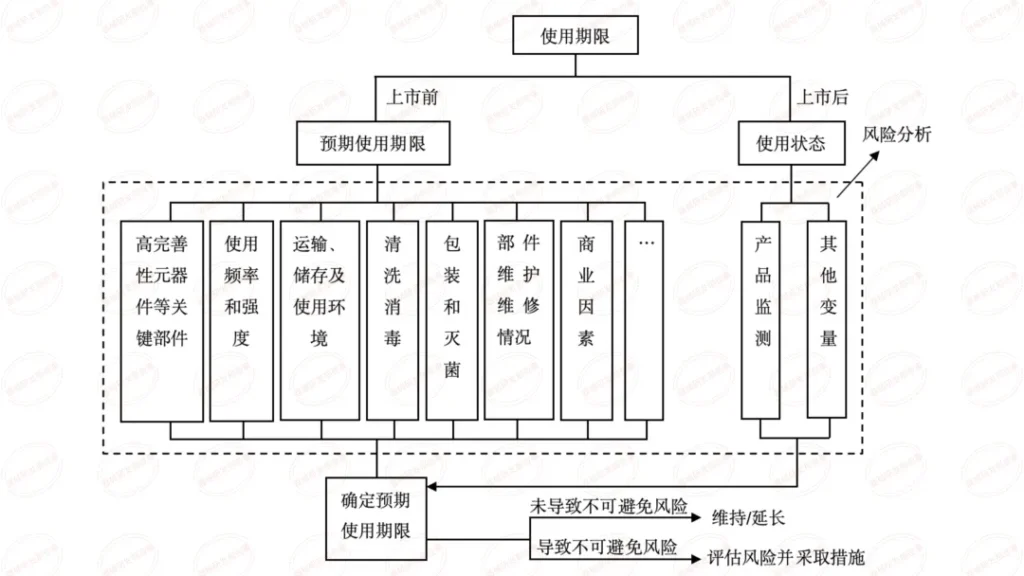
本篇内容为学习总结,源自审评二部陈敏老师关于《有源医疗器械注册申报资料要求及常见问题介绍》在器审中心学习云课程的视频。陈老师主要介绍了共性问题、研究资料-联合使用、研究资料-生物学特性、研究资料-清洁、消毒、灭菌、稳定性和92个技术审评共性问题等六个方面。






