一、引言
由医疗质量检测技术及测试仪器展知悉,本规范基于《医药工业洁净厂房设计规范》,进一步细化了医疗器械生产洁净室的验证管理要求,特别是设计计划(DQ)、安装验证(IQ)、运行验证(OQ)和性能验证(PQ)四个关键阶段,以确保洁净室的设计、建设、运行均符合GMP及国家相关标准,保障医疗器械的生产质量和安全性。
二、适用范围
本规范适用于所有涉及医疗器械生产的洁净室,包括无菌医疗器械、直接接触药品的包装材料等生产环境的新建、改建和扩建项目。
三、基本原则
1.技术先进、确保质量:洁净室设计应采用先进技术,确保产品质量稳定可靠。
2.安全实用、经济合理:设计需考虑安全性、实用性和经济性,符合节约能源和保护环境的要求。
3.符合法规、持续改进:遵循国家相关法律法规及GMP要求,并根据生产发展和工艺改进需要不断优化。
洁净室(区)综合性能评定检测项目
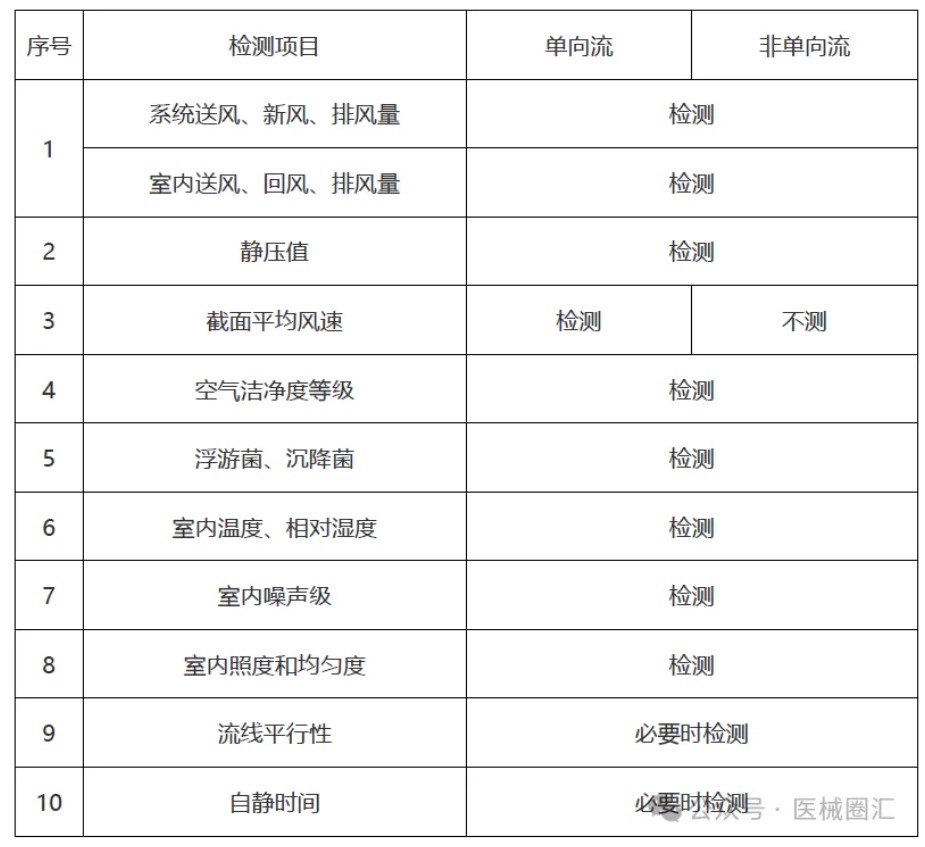
图片来源:医械圈汇
四、验证管理内容(一)
1. 设计计划验证(DQ)
·用户需求分析:明确洁净室的使用目的、产品特性、生产工艺要求及GMP规范等,形成详细的设计需求。
·设计文件审查:审查洁净室的设计图纸、技术规格书、材料清单等文件,确保其符合设计需求及相关法规标准。
·风险评估:对设计进行风险评估,识别潜在的设计缺陷或不符合项,并提出改进措施。
2. 安装验证(IQ)
·设备检查:检查所有安装的设备、管道、阀门等是否符合设计要求及制造商标准。
·安装记录:记录安装过程中的关键步骤、使用的工具、材料以及任何异常情况。
·校准与测试:对关键设备进行校准和测试,确保其性能符合设计要求。
3. 运行验证(OQ)
·系统调试:在洁净室空载状态下,对空气净化系统、温湿度控制系统、压差控制系统等进行调试,确保各系统正常运行。
·操作程序验证:验证洁净室的操作程序是否完善、合理,操作人员是否熟悉并能正确执行。
·模拟运行:模拟实际生产过程,验证洁净室在动态条件下的稳定性和可靠性。
4. 性能验证(PQ)
·环境参数监测:连续监测洁净室内的微粒、微生物、温度、湿度、压差等环境参数,确保其符合设计要求及GMP标准。
·产品试生产:在洁净室内进行产品试生产,验证生产环境对产品质量的影响。
·持续监测与评估:建立持续监测机制,定期评估洁净室的性能,并根据评估结果采取必要的改进措施。
五、验证管理内容(二)
1. 洁净室设计验证
·环境参数设计:根据《医药工业洁净厂房设计规范》,明确洁净室的环境参数,包括微粒和微生物控制、温度、湿度、新鲜空气量、压差、照度、噪声等。
·空气洁净度等级:根据产品特性和生产工艺要求,确定洁净室的空气洁净度等级,并进行验证。
·布局合理性:验证洁净室的布局是否合理,防止人流、物流交叉污染,确保生产流程顺畅。
2. 设施与设备验证
·空气净化系统:验证空气净化系统的性能,包括过滤效率、送风量、回风量、排风量等,确保满足洁净度要求。
·压差控制系统:验证洁净室与非洁净区、不同洁净度等级区域之间的压差控制是否有效,防止污染。
·温湿度控制系统:验证温湿度控制设备的稳定性和准确性,确保生产环境满足工艺要求。
3. 验证过程
·静态验证:在洁净室空载状态下进行,主要验证空气洁净度、压差、温湿度等环境参数是否达标。
·动态验证:在洁净室正常运行状态下进行,模拟实际生产过程,验证各项环境参数和生产设备的稳定性和可靠性。
·微生物监测:定期进行微生物监测,确保洁净室内无有害微生物污染。
4. 验证报告与记录
·验证报告:每次验证结束后,应编制详细的验证报告,包括验证目的、方法、结果、结论及建议等。
·记录管理:建立验证记录管理制度,确保所有验证记录真实、完整、可追溯。
五、维护与持续改进
·日常维护:定期对洁净室进行清洁、消毒和维护,确保各项设施和设备处于良好状态。
·定期复验:根据产品特性和生产需求,定期对洁净室进行复验,确保持续符合GMP要求。
·持续改进:根据验证结果和生产经验,不断优化洁净室的设计和管理,提高生产效率和产品质量。
(一)洁净室(区)运行管理
1.空调系统的使用规定:应包括工作前的开机时间、中断一定时间的再使用的自净时间的规定—必要时具备验证报告。
2.确定环境检测的项目、指标、频次、方法:内容参见《无菌医疗器具生产质量管理规范》(YY0033-2000)。
3.洁净室(区)的卫生(清洗、消毒)管理规定:应包括车间里的空气、墙、台面、工位器具、周转箱等的清洗或消毒方法和频次以及洁具的管理。
4、洁净室(区)的物流管理规定:应包括物料进出洁净室(区)的规定。
5、净化车间里的人员卫生管理规定:应包括人员进出以及在净化车间中的卫生管理规
定以及服装清洗消毒的管理。
(二)洁净室(区)日常维护
1.定期进行空调机组设备的维护和保养:包括空调系统的检修、以及相关部件的维护管理,如可能的电机、传感器等。
2.定期对空调机组的功能进行检测和保养:对初、中、高效过滤器的保养,包括清洗、更换。
3.空调机组功效的维护:可通过送风量的大小(换气次数)进行监测。
4.配套空调机组使用的其他设备的管理:如空气净化器、臭氧消毒器等的管理。
六、附录
·名词解释:对规范中涉及的专业术语进行解释。
·本规范用词说明:明确规范中使用的词汇和表述方式的含义和范围。
七、结语
通过实施设计计划验证(DQ)、安装验证(IQ)、运行验证(OQ)和性能验证(PQ)这一系列严谨的验证流程,可以确保医疗器械生产洁净室的设计、建设、运行均达到预定目标,满足GMP及国家相关标准的要求。各生产企业应严格按照本规范进行验证管理,不断提升洁净室的管理水平,为医疗器械的生产提供安全、可靠的环境保障。
想要了解更多请前往医疗质量检测技术及测试仪器展
文章来源:医械圈汇
若涉及侵权,请立刻联系删除
关键字:









