1.前言
山东省医疗器械洁净室(区)现场检查指南(2021版)
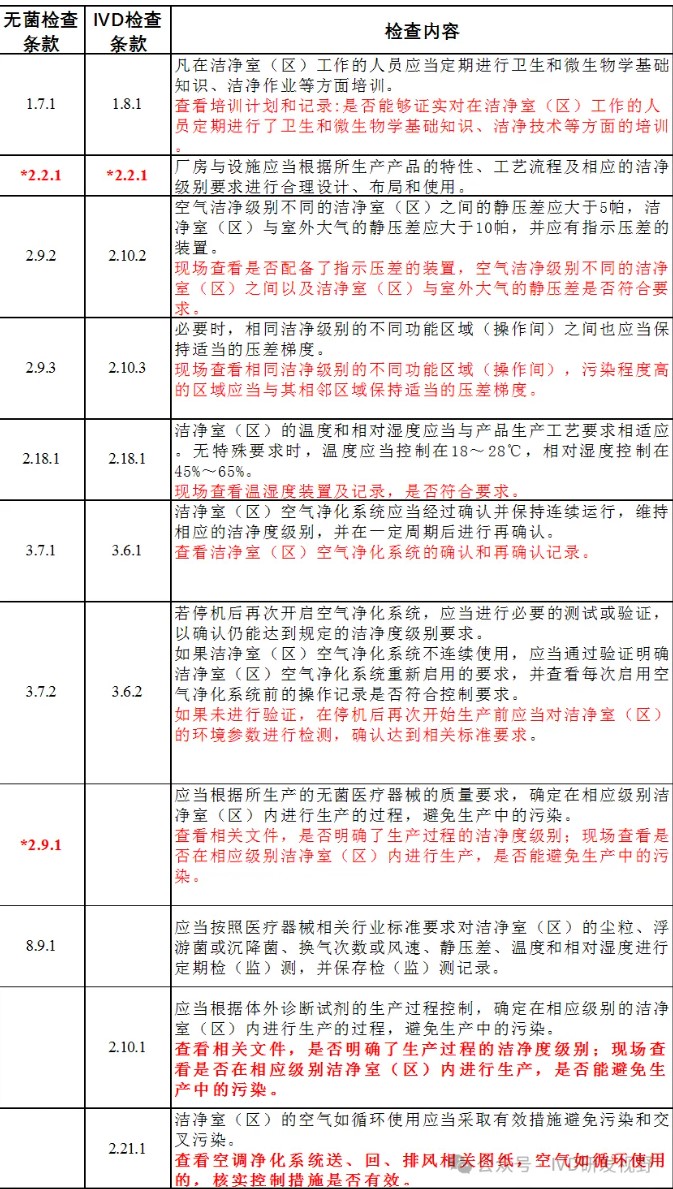
2.GMP的要求
《医疗器械生产质量管理规范附录无菌医疗器械》、
《医疗器械生产质量管理规范附录体外诊断试剂》、
《医疗器械生产质量管理规范体外诊断试剂现场检查指导原则》、
《医疗器械生产质量管理规范无菌医疗器械现场检查指导原则》、
图片来源:IVD研发视野
3.常见飞检不符合项

图片来源:IVD研发视野
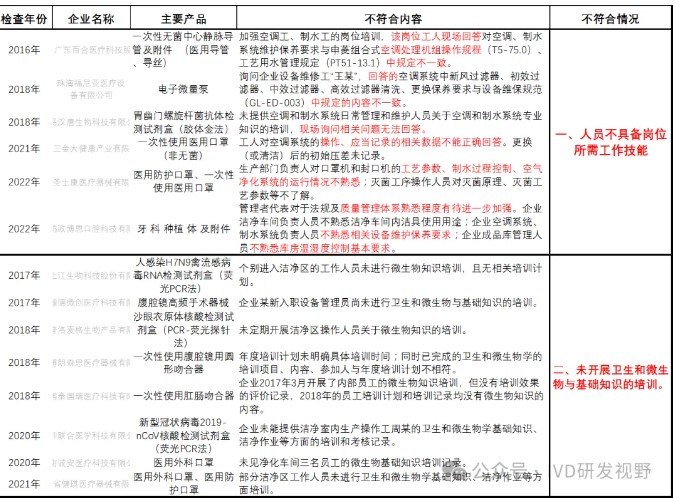
一、人员不具备岗位所需工作技能
二、未开展卫生和微生物与基础知识的培训
图片来源:IVD研发视野
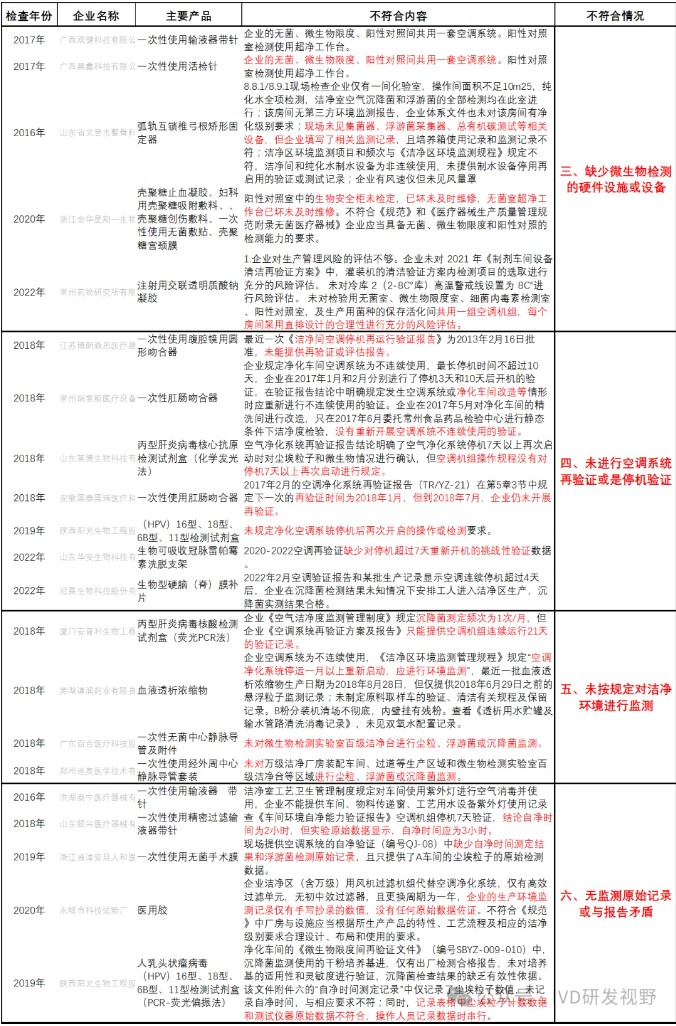
三、缺少微生物检测的硬件设施或设备
四、未进行空调系统再验证或是停机验证
五、未按规定对洁净环境进行监测
六、无监测原始记录或与报告矛盾
图片来源:IVD研发视野
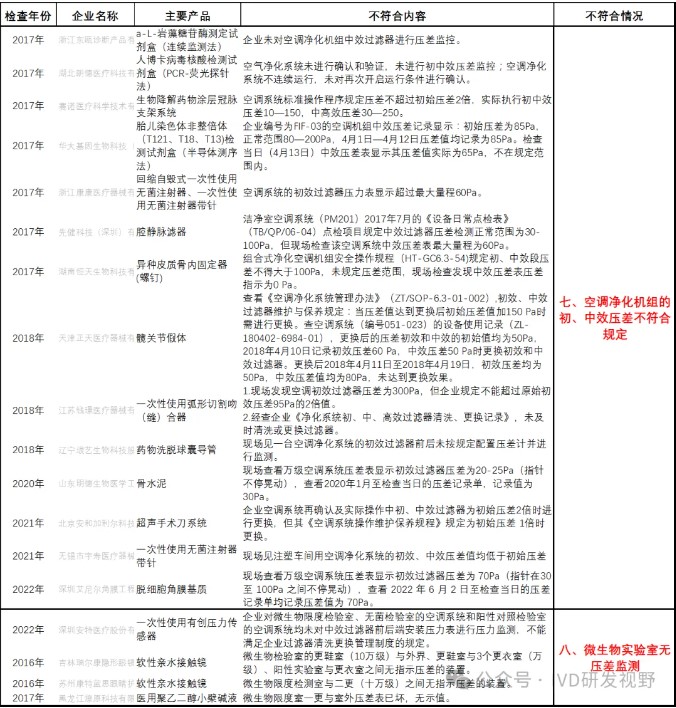
七、空调净化机组的初/中效压差不符合规定
八、微生物实验室无压差监测
图片来源:IVD研发视野
九、设备未定期校准
十、未制定维护保养规定或未执行
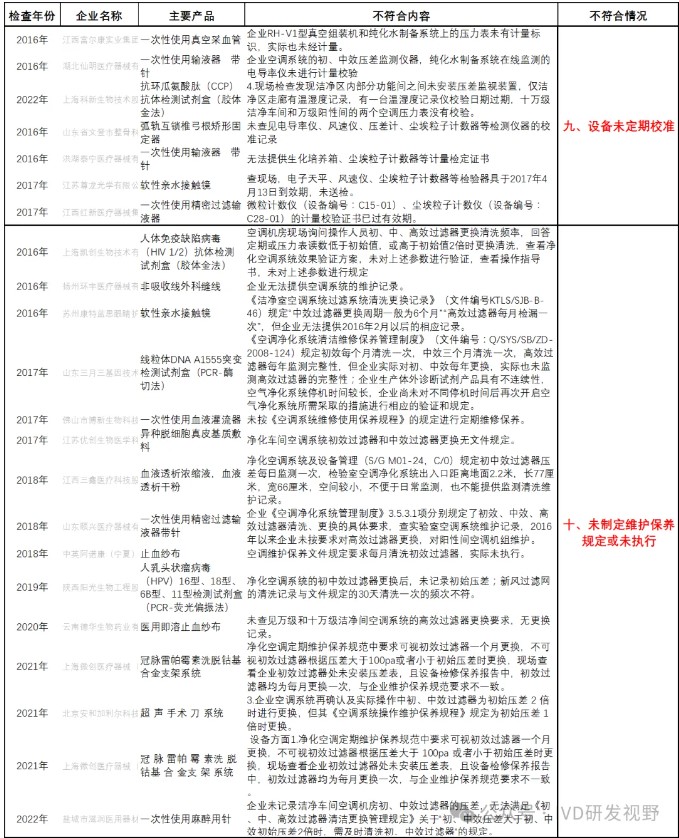
图片来源:IVD研发视野
4.结语
想要了解更多请前往医疗质量检测技术及测试仪器展
文章来源:IVD研发视野
若涉及侵权,请立刻联系删除
关键字:









